(2025年3月1日作成)
○原因と背景
○感染経路と症状
○奈良県における薬剤耐性菌による感染症年次別報告数
○奈良県保健研究センターにおける耐性遺伝子検査状況
○薬剤耐性化とその対策
○最後に
○参考
薬剤耐性菌とは、治療に使用する特定の種類の抗菌薬(抗生物質)が効きにくい、または効かなくなった細菌です。複数の抗菌薬に耐性を示す「多剤耐性菌」や、「最後の切り札」とされるカルバペネム系抗生物質に耐性を示す腸内細菌目細菌(CRE)の出現・増加など、世界中で問題となっています。
「薬剤耐性菌に起因する死亡者は約70万人(2013年)、このまま、何も対策を取らない場合、2050年にはガンによる死亡者を超えて1000万人に達する」(オニールレポート)とされ、薬剤耐性(AMR)に関するグローバルアクションプランが2015年にWHO総会で採択されました。
日本では2016年からAMR対策アクションプランが開始され、ヒト・動物・環境の多分野で取り組む、包括的な対策「ワンヘルス・アプローチ」が提唱されています。
◎厚生労働省におけるAMRの取組について(厚生労働省)
◎薬剤耐性(AMR)対策について(厚生労働省)
薬剤耐性菌はヒトからヒト、ヒトから環境へと拡がります。特に、抗菌薬使用が不可欠な患者が多く入院する医療機関では、医療従事者の手指や医療器具等を介し、拡がってしまうことがあります。さらに、近年では、医療行為を受けていないヒトに感染する市中感染症も増加しています。
薬剤耐性菌は、病原性の弱い常在菌の場合が多く、一般的に、感染しても保菌状態のまま、無症状で経過します。しかし、免疫が低下している患者や高齢者等では、薬剤耐性菌が血中に侵入し、症状を呈することがあります。症状は、薬剤耐性菌が定着する臓器や器官によって様々です。
薬剤耐性菌による感染症のうち、臨床的に重要な7疾患を下記に示します。これらの感染症は、感染症法に基づき、届出の対象となっています。
|
◆五類全数把握(4 疾患)
*カルバペネム耐性腸内細菌目細菌(CRE)感染症
*バンコマイシン耐性腸球菌(VRE)感染症
*バンコマイシン耐性黄色ブドウ球菌(VRSA)感染症
*薬剤耐性アシネトバクター(MDRA)感染症
|
|
◆五類定点把握(3 疾患)
*メチシリン耐性黄色ブドウ球菌(MRSA)感染症
*ペニシリン耐性肺炎球菌(PRSP)感染症
*薬剤耐性緑膿菌(MDRP)感染症
|
◎薬剤耐性菌感染症について(国立感染症研究所)
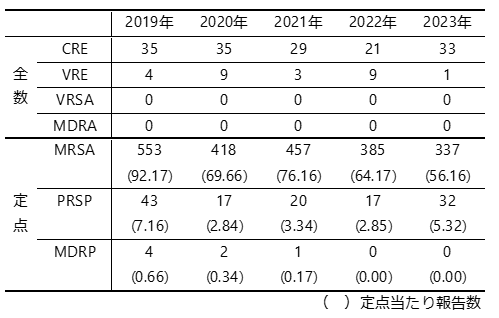
CRE、VREについては、厚生労働省通知(健感発0328第4号)により、奈良市を含む県内全医療機関の届出患者より分離した菌株を対象に、耐性遺伝子検査を実施しています。解析結果に関する詳細は、奈良県保健研究センター年報をご覧ください。
細菌は様々な方法で抗菌薬を無効にしようと試みます。耐性のメカニズムは様々で、細菌が本来もっているもの、他の細菌から譲り受けるもの、抗菌薬投与により誘導されるものがあります。
このうち、抗菌薬投与により誘導され、耐性化する原因として、抗菌薬の不適正な使用があげられます。必要のない抗菌薬を使用することで、体内にいる細菌がその抗菌薬への耐性をもつ可能性が高くなります。また、指示された服用方法を変更してしまうと、生き残った細菌から耐性菌が出現することがあります。薬剤耐性菌をふやさないために、抗菌薬を使用する際は、下記の3つのポイントを守りましょう。
*抗菌薬は医師の指示どおり服用しましょう
処方された抗菌薬は、医師の指示どおり、量・期間を守って服用しましょう。症状が治まったからといって服用を中断しないようにしましょう。
*抗菌薬はウイルスには効きません
風邪やインフルエンザなどウイルスによって起こる感染症には抗菌薬は効きません。症状がある時は、以前に処方された抗菌薬を自己判断で服用せず、医療機関を受診しましょう。
*基本的な感染症対策をしましょう
日々の手洗い・うがいを心がけ、必要なワクチンを接種し、予防できる感染症にかからないようにしましょう。
1928年のフレミングによるペニシリンの発見から、新しい抗菌薬の開発が進んだことで、多くの感染症が激減しました。しかし、抗菌薬が使われるようになるとそれに対する耐性菌が出現します。また、抗菌薬の開発には莫大なコストと時間がかかるため、新しい抗菌薬がほとんど出てこない状況に陥っています。菌の薬剤耐性化が進む一方、抗菌薬の開発が停滞すると、耐性菌による感染症にかかった場合に、治療が大変厳しい状況になります。このような事態を避けるためには、抗菌薬を正しく使い、現在使える抗菌薬を長く使えるようにすることが大切です。
・AMR臨床リファレンスセンター
・感染症発生動向調査事業年報確定報告データ(厚生労働省健康・生活衛生局感染症対策部感染症対策課、国立感染症研究所感染症疫学センター、2018年~2022年)
・感染症発生動向調査週報 速報データ(2023年)
(文責 細菌担当)